Medizinprodukterecht-Durchführungsgesetz (MPDG): Überblick zu aktuellen Neuerungen und Hinweise zur Anwendung
14.10.2021 | FMC – Online-Redaktion, Forum Verlag Herkert GmbH
Am 26.05.2021 ist das Medizinprodukterecht-Durchführungsgesetz (MPDG) in Kraft getreten. Allerdings treten bis Mai 2022 noch weitere Änderungen in Kraft. Die umfassenden Anpassungen wirken sich massiv auf das bislang geltende Medizinproduktegesetz und weitere Vorschriften aus. Doch was ändert sich mit dem MPDG? Worauf müssen Ärzte, Krankenhäuser, Therapeuten und Medizinprodukthersteller achten?
Inhaltsverzeichnis
- Überblick: Neuerungen durch MPDG am Medizinproduktegesetz
- Welche Bedeutung hat das MPDG konkret?
- Beispiele für Medizinprodukte nach dem Medizinprodukterecht-Durchführungsgesetz
- Vorgaben des MPDG rechtssicher umsetzen
Überblick: Neuerungen durch MPDG am Medizinproduktegesetz
Grundlage des MPDG ist das Inkrafttreten der Europäischen Medizinprodukteverordnung (Medical Device Regulation, MDR). Diese bewirkt zahlreiche Änderungen am Medizinproduktegesetz (MPG) und vielen Richtlinien. Der folgende Abschnitt gibt einen Überblick über die wichtigsten Neuerungen.
Grundlegende Änderungen durch Medizinprodukterecht-Durchführungsgesetz
Im Vergleich zu den bisherigen Regelungen durch das Medizinproduktegesetz ergeben sich mit dem MPDG diese wesentlichen Neuerungen:
- Grundlegende Vorgaben und Anforderungen sind nicht mehr gesondert in anderen Vorschriften nachzulesen. Sie sind nun ebenfalls im MPDG enthalten.
- Spezifische nationale Anforderungen, die über die EU-Vorgaben hinausreichen, sind ebenfalls aufgeführt.
- Die zuständigen Behörden in Deutschland tragen mehr Verantwortung.
- Es gelten erweiterte bzw. verschärfte Strafmaß- und Bußgeldkataloge bei Verstößen gegen das MPDG.
 |
| Das Medizinprodukterecht-Durchführungsgesetz sorgt für mehr Klarheit und Transparenz in den verschiedenen Vorschriften. EU-Vorgaben werden dabei in nationales Recht übertragen und teils verschärft. Strenges QM und sorgfältige Dokumentation helfen bei der Umsetzung der Vorgaben. Bild: © yavdat – stock.adobe.com |
Geänderte Vorschriften durch Medizinprodukte-Anpassungsgesetz
Als Begleitgesetz zum MDR sorgt das Medizinprodukte-Durchführungsgesetz (MPDG) für mehr Transparenz:
- Neufassung notwendiger Abschnitte
- Entfernen redundanter Abschnitte
- Bündelung der Vorgaben in zentrale Gesetze für Medizinprodukte (Beispiele unten)
Gleichzeitig regelt das Medizinprodukterecht-Durchführungsgesetz auf Bundesebene folgende Punkte:
- Zuständigkeit von Behörden in den einzelnen Ländern
- Strafmaß bei Verstößen gegen MPDG-Vorgaben (Freiheitsstrafen, Bußgelder)
- Spezifische nationale Anforderungen
Eine zentrale Rolle spielt hierbei das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), da es folgende Befugnisse hat:
- Es steuert die zuständigen Landesbehörden.
- Es verfügt über verschiedene Möglichkeiten, bei Gefahr in Verzug zu handeln. Diese kann etwa von bereits vertriebenen Medizinprodukten mit CE-Kennzeichnung ausgehen.
- Das Institut betreibt das Deutsche Medizinprodukte-Informations- und Datenbanksystem (DMIDS). Damit erhält und bewertet es Anzeigen und Anträge im Medizinproduktebereich.
- Es verwaltet die diesbezügliche Schnittstelle u. a. zur europäischen Medizinprodukte-Datenbank EUDAMED.
Wichtig: Einrichtungen des Gesundheitswesens sollten die Änderungen im Rahmen des MPDG und seine Einhaltung genauestens prüfen. Für sie können neue Pflichten und Anforderungen entstanden sein, die unter dem Medizinproduktegesetz zuvor nicht bestanden. So müssen sich künftig z. B. Unternehmen, die sich mit der Aufbereitung von Medizinprodukten befassen, behördlich registrieren.
Welche Bedeutung hat das MPDG konkret?
Die Änderungen durch das MPDG erschweren den Überblick über aktuelle Vorgaben rund um die MDR und das Medizinproduktegesetz. Eine Definition und ein Kurzüberblick ermöglichen ein schnelleres Erfassen der zentralen Punkte.
Was ist das Medizinprodukte-Durchführungsgesetz (MPDG)?
Das „Gesetz zur Durchführung unionsrechtlicher Vorschriften betreffend Medizinprodukte“, auch „Medizinprodukte-Durchführungsgesetz“ oder „MPDG“ löst das bis zum Jahr 2021 gültige Medizinproduktegesetz (MPG) ab.
Die zentralen Ziele des neuen Gesetzes sind:
- Regeln des Verkehrs von Medizinprodukten
- Gewährleisten der Sicherheit, Eignung und Leistung der Produkte
- Sicherstellen des Schutzes von Patienten, Anwendern und Dritten
Der Gesetzestext des MPDG umfasst insgesamt zehn Kapitel:
- Zweck, Anwendungsbereich und Begriffsbestimmungen
- Anzeigepflichten, Inverkehrbringen und Inbetriebnahme von Produkten sowie deren Bereitstellung auf dem Markt, sonstige Bestimmungen
- Benannte Stellen, Prüflaboratorien, Konformitätsbewertungsstellen für Drittstaaten
- Klinische Prüfungen und sonstige klinische Prüfungen
- Vigilanz und Überwachung
- Medizinprodukteberater
- Zuständige Behörden, Verordnungsermächtigungen, sonstige Bestimmungen
- Sondervorschriften für den Bereich der Bundeswehr und den Zivil- und Katastrophenschutz
- Straf- und Bußgeldvorschriften
- Übergangsbestimmungen
Das Medizinprodukte-Durchführungsgesetz wurde am 28.04.2020 erlassen. In großen Teilen ist es am 26.05.2021 in Kraft getreten. Die letzte Änderung vom 12.05.2021 tritt zum 26.05.2022 in Kraft. Sowohl die MDR als auch das MPDG wurden aufgrund der Corona-Pandemie von April 2020 auf Mai 2021 verschoben.
Nationales Recht überträgt, präzisiert und verschärft die Vorgaben der EU
Das MPDG stellt eine Übertragung von Vorgaben und Anforderungen an Medizinprodukte auf europäischer Ebene in nationales Recht dar. Diese Übertragung betrifft in erster Linie:
- Aktive implantierbare medizinische Geräte (90/385/EWG)
- Medizinprodukte (93/42/EWG)
- In-vitro-Diagnostika (98/79/EG)
Zu diesen Vorgaben kommen weitere nationale Vorschriften hinzu, etwa zum Inverkehrbringen von Medizinprodukten. Sie betreffen darüber hinaus insbesondere die folgenden Aspekte:
- Überwachung,
- Betreiben,
- Anwendung, sowie
- Instandhaltung von Medizinprodukten
Bisherige Gesetze und Regelungen werden abgelöst
Mit dem Medizinprodukterecht-Durchführungsgesetz treten bis Mai 2022 diese Verordnungen vollständig außer Kraft:
- Medizinprodukte-Verordnung (MPV)
- Verordnung über klinische Prüfungen von Medizinprodukten (MPKPV)
Andere Vorschriften werden abgelöst:
- Medizinprodukte-Gebührenverordnung (MedProdGebV)
→ Sie wird durch eine nationale Rechtsverordnung abgelöst. - Medizingeräteverordnung (MedGV)
→ Sie war zuvor nur für medizinisch-technische Geräte gültig. Das MPDG beinhaltet nun einheitliche Begriffsbestimmungen und Regelungen für Medizinprodukte.
Beispiele für Medizinprodukte nach dem MPDG
Medizinprodukte werden zur medizinischen Anwendung am Menschen hergestellt. In diesem Zuge behandelt § 3 MPDG folgende Produkte:
- Medizinprodukte
- Zubehör der Medizinprodukte
- Produkte aus Anhang XVI der Verordnung (EU) 2017/745
Mit dieser medizinischen Zweckbestimmung lassen sich leicht die folgenden Beispiele als Medizinprodukte klassifizieren:
- Implantate
- Verbandsstoffe
- Dentalprodukte
- Herzschrittmacher
- Injektionsprodukte
- Ärztliche Instrumente
- Geräte zur Untersuchung
Auch In-vitro-Diagnostika zählen zu Medizinprodukten, obgleich diese nicht wie andere Medizinprodukte einer Klasse zugeordnet werden. Beispiele hierfür sind:
- Reagenzprodukte
- Probenbehältnisse
- Geräte zur Probenuntersuchung
Laut Definition von Medizinprodukten nach dem Bundesgesundheitsministerium geht es bei Medizinprodukten vorrangig um deren physikalische Eigenschaften. Gemeint ist hiermit die bestimmungsgemäße Hauptwirkung. Im Gegensatz dazu zeichnen sich z. B. Arzneimittel durch nicht-physikalische Wirkungsweisen aus, sondern wirken pharmakologisch, immunologisch und metabolisch.
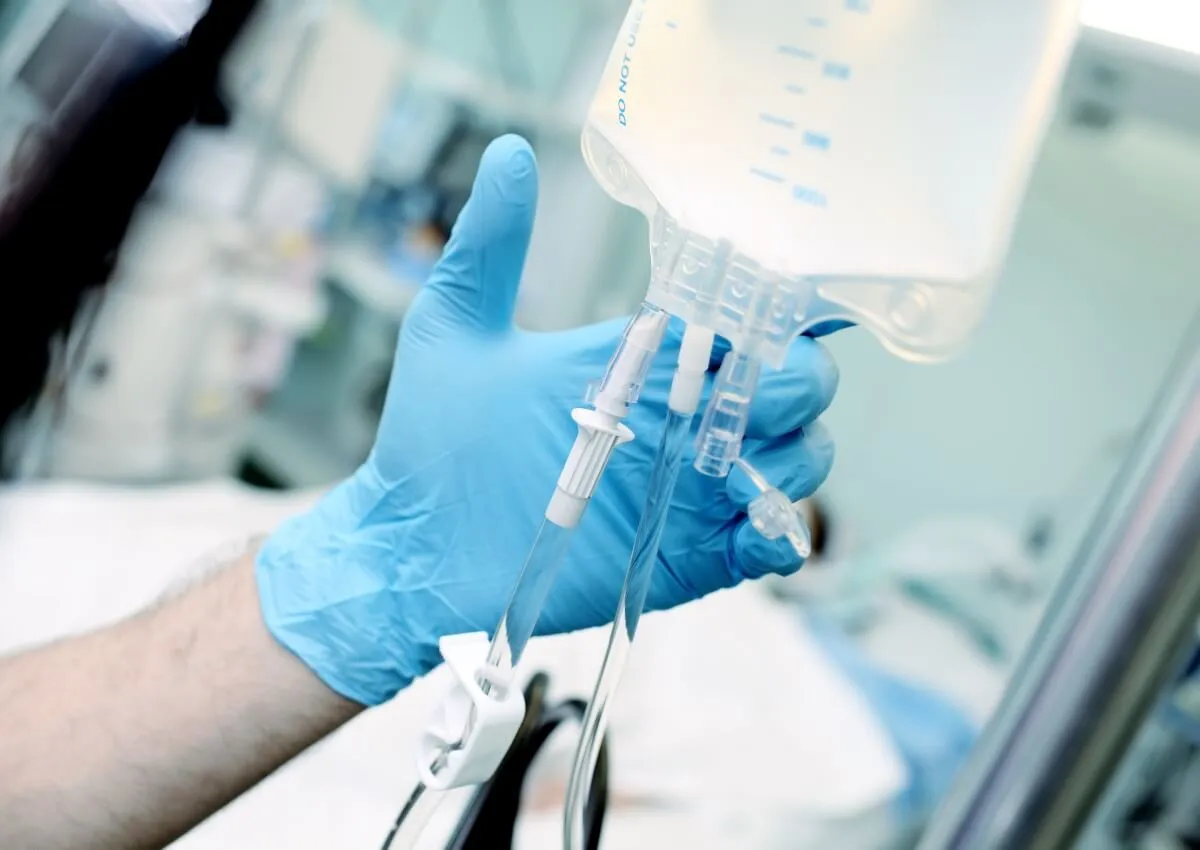
 |
| Die Zweckbestimmung von Medizinprodukten, die unter das Medizinprodukterecht-Durchführungsgesetz (MPDG) fallen, betrifft auch jene zur humanmedizinischen Untersuchung von Proben und Flüssigkeiten. Mit dem vollständigen QM-Handbuch „SicherheitsCheck Qualitätsmanagement, Arbeitssicherheit und Hygiene“ behalten Einrichtungen des Gesundheitswesens den Überblick über alle geltenden Vorschriften. Bild: © Gorodenkoff – stock.adobe.com |
Vorgaben des MPDG rechtssicher umsetzen
Mit dem Medizinprodukterecht-Durchführungsgesetz hat die Bundesregierung EU-Vorschriften in nationalem Recht verankert. Gleichzeitig soll es für mehr Transparenz in den verschiedenen Bereichen des Medizinprodukterechts sorgen. Allerdings wurden die Vorgaben verschärft, sodass auf Gesundheitseinrichtungen und Unternehmen neue Vorschriften und Pflichten zukommen.
Verantwortliche in den Unternehmen, aber auch Ärzte, Therapeuten und Pflegeeinrichtungen müssen dabei stets den Überblick über aktuelle Vorschriften bewahren. Sie müssen sicherstellen, dass sie sämtliche aktuelle Anforderungen erfüllen und sorgfältig dokumentieren.
Produktempfehlung
Eine hilfreiche Stütze bei diesem Vorhaben ist das Handbuch „SicherheitsCheck Qualitätsmanagement, Arbeitssicherheit und Hygiene“. Es bietet einen verständlichen Überblick über alle aktuellen Anforderungen sowie ein fertiges Muster-QM-Handbuch zum individuellen Anpassen. Jetzt bestellen!
Quellen: „SicherheitsCheck Qualitätsmanagement, Arbeitssicherheit und Hygiene“, Medizinprodukterecht-Durchführungsgesetz, bundesgesundheitsministerium.de, bfarm.de